Nanopartículas, unha ferramenta prometedora contra o cancro
A primeira vista un podería pensar que se trata dun conto tecnolóxico más, dunha farsa, dun charlatán de feira ou simplemente un grandilocuente científico. Non obstante, o Dr. Hainfeld é un recoñecido investigador de prestixio internacional e un dos creadores destas nanopartículas alá polos anos 70 no Laboratorio Nacional de Brookhaven (EE.UU.).
Nanopartículas de ouro
Todos nós somos coñecedores do uso do ouro en la xoiería ou na fabricación de compoñentes electrónicos, aínda que a maoría ignoramos a súa aplicación no campo de la medicina. Na cultura china xa se empregaba o ouro na elaboración de remedios 2500 a.C. Na medicina moderna ségunse utilizando compostos de ouro como antiinflamatorios no tratamiento da artrite reumatoide e outras enfermidades reumáticas; aínda que actualmente ten despertado grande interese polas súas posibles aplicacións médicas un tipo particular de ouro, as nanopartículas de ouro.A razón pola cal as partículas de ouro son moi utilizadas no ámbito da medicina débese a que este metal non reacciona o reacciona moi pouco con otras substancias, sendo un material compatible coa vida e bo candidato, posto que usando unha cantidade terapéutica de nanopartículas cabe esperar que non orixine toxicidade, coágulos, cancro ou otras complicacións. Outra característica favorable das nanopartículas de ouro é que son relativamente sinxelas de sintetizar e manipular, permitindo a obtención dunha grande diversidade de formas, por exemplo, esferas, cilindros, tubos, caixas, entre outras. Por outro lado, o ouro pode formar fácilmente unións estables con xofre, carbono, flúor, cloro, bromo, iodo e outros elementos; gracias a isto pódeselle unir moléculas de orixe biolóxica para conferir ás nanopartículas de ouro múltiples propiedades físico-químicas e biolóxicas (por exemplo, anticorpos).
Nanopartículas e fármacos
Unha das aplicacións máis ambiciosas e de maior difusión das nanopartículas de ouro é o transporte de fármacos, xa sexa acoplados á súa superficie, xa sexa encapsulados; tal é ó caso das cestas (nanoshells), nanopartículas de ouro construidas cun oco no centro, as cales teñen demostrado ser un excelente transportador de fármacos; uso que permite aumentar a solubilidade destes favorecendo o seu paso a través das membranas celulares. Xa existen varios medicamentos basados neste sistema de transporte de fármacos, entre os cales pódese citar algúns xa clásicos como o Daunoxome® (Diatos) para o tratamento de leucemias e Sarcoma de Kaposi, Doxil® (Johnson & Johnson) para o tratamento de carcinoma de ovario ou Abraxane® (Ameristat Pharmaceuticals Inc.) para o tratamento do cancro de mama. As nanopartículas de ouro tamén poden utilizarse para ser activadas por cambios no pH ou mediante estímulos químicos e, así, controlar a velocidade de liberación do fármaco e, mesmo, para dirixir o fármaco cara unha célula en particular, mediante a adición de anticorpos específicos. O anterior evita que o fármaco se distribuia en tódolos tecidos e órganos do corpo, para alcanzar só aqueles onde debe ter efecto, e permite diminuir as doses administradas, reducindo os efectos adversos e a fluctuación da súa concentración no sangue cun efecto terapéutico máis uniforme.Nanopartículas e diagnóstico
Outro dos usos máis prometedores a curto prazo é o uso de nanopartículas de ouro de 15nm como contraste radiolóxico, ofrecendo un inmellorable alto contraste (aproximadamente 3 veces maior có iodo e sen dano vascular) e cunha longa permanencia no sangue (vida media de 24 horas, co cal é posible repetir o estudio varios días despois da súa administración). Ademais como non é tóxico (LD50 >5.0 g Au/kg), pódese volver a explorar os animais (de momento o seu uso só está aprobado en animais de laboratorio) máis tarde para estudiar a progresión dun cancro ou unha enfermidade vascular ó longo do tempo.
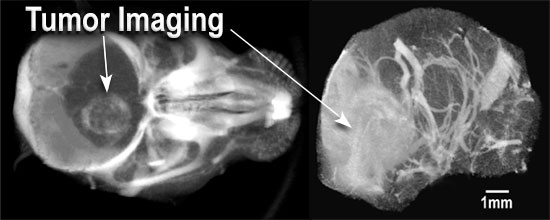
Estas nanopartículas, acopladas con moléculas de gadolinio (Gd), presentan a vantaxe de ser detectables tanto no TC (gracias ó Au) como na RM (Gd). Estos nuevos axentes de contraste ofrecen a posibilidade de localizar un tumor cando o seu tamaño é pequeno e antes dos primeros síntomas.
Nanopartículas e radioterapia
Ademais do uso destas nanopartículas no transporte orientado de quimioterápicos ou ben como portadoras de xens (para o tratamento do Parkinson, Alzheimer, etc.), está de plena actualidade a súa utilización en hipertermia e radioterapia como radiosensibilizadores (isto é, para incrementar a dose efectiva administrada). A hipertermia é unha técnica experimental que consiste no uso de fontes de calor co obxecto de obter un aumento da temperatura no interior do organismo, ben sexa por medio de fármacos ou aparatos médicos (p.ex. a ablación por radiofrecuencia). Este mecanismo de elevación da temperatura local pódese empregar para o tratamento dalgúns tipos de cancros en combinación coa radioterapia e/ou quimioterapia, dado que consegue mellorar a sensibilidade da célula tumoral ó efecto radioterapéutico e quimioterapéutico ó danar as súas proteínas de membrana e inhibir tamén a reparación do ADN celular danado. A hipertermia magnética, ou inxección de nanopartículas magnéticas nun tumor, é un novo método experimental para o tratamento de certos cancros, en especial os de próstata e cerebro. O tratamento de hipertermia magnética consiste en inxectar directamente nanopartículas magnéticas a un tumor. O paciente é entón introducido nunha máquina que produce un campo magnético alterno provocando que as nanopartículas oscilen e produzan calor no interior do tecido tumoral. Cando a temperatura se eleva por riba de 42º C, as células cancerosas comezan a morrer. Demostrouse que este proceso reduce o tamaño dos tumores, pero aínda se desconoce cal é o mecanismo biolóxico concreto. Tamén se descoñece cal sería a dose ou a duración adecuadas.Nos anos 50 do século pasado xa se observou en radioloxía intervencionista certa radiosensibilidade na presenza de axentes de contraste (iodo) durante os cateterismos.Nos años 80 o brasileiro Renato Santos Mello estudiou como a concentración de iodo aumentaba a dosis de radiación absorbida a partir de fontes de raios X ou fotóns gamma de baixa enerxía. Hai poucos anos distintos científicos usaron as nanopartículas para investigar este mesmo efecto de intensificación da dose de radiación.
 |
Estes gráficos pretenden ilustrar os mecanismos de interacción dos raios-X coas nanopartículas de alto número atómico Z (Esquerda) e deposición da enerxía na escala das nanopartículas de ouro baixo a irradiación de raios-X (Dereita). Tres efectos combínanse neste fenómeno: a absorción local de raios-X polas nanoestructuras (efecto fotoeléctico), a liberación de electróns de baixa enerxía (electróns Auger) desde as nanopartículas, e a deposición de enerxía na agua en forma de radicais e electróns. Non obstante, hai outros mecanismos bioquímicos moi relevantes debidos a estas nanopartículas metálicas que aínda están en fase de estudio e investigación co fin de explicar a gran potenciación da resposta biolóxica ás doses de radiación na súa presenza.
Fontes: Deep Kwatra, Anand Venugopal, Shrikant Anant "Nanoparticles in radiation therapy: a summary of various approaches to enhance radiosensitization in cancer", Translational Cancer Research, 2013 y Carter, J. D.; Cheng, N. N.; Qu, Y.; Suarez, G. D.; Guo, T. "Nanoscale Energy Deposition by X-ray Absorbing Nanostructures", The Journal Physical Chemistry Letters 2007.
|
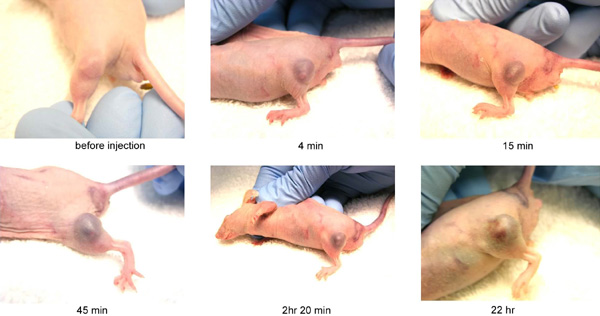
Un dos experimentos pioneiros neste campo foi levado a cabo polo equipo do profesor Hainfeld no ano 2004, no cual inxectaron nanopartículas de ouro en tumores subcutáneos en ratos en distintas concentracións para estudiar o seu efecto na irradiación posterior de 30Gy con raios-X de 250 kVp.
Tal como mostran os seguintes gráficos, observouse un aumento espectacular da supervivencia nun factor 4 en presenza de nanopartículas de ouro de 2nm de diámetro en concentracións de 2,7 mg/ml. Os procesos detrás deste aumento de muerte celular son complexos e todavía non hai unha explicación clara dos resultados observados experimentalmente.
|
Futuro
Actualmente, unha cantidad crecente de productos terapéuticos fabricados a base de nanopartículas encóntrase en estudio clínico, varios dos cales foron xa introducidos no mercado e é moi probable que esta tendencia siga en aumento, debido a que as nanopartículas permiten a implementación de medidas terapéuticas de maneira máis eficaz, pois son ferramentas con gran bioafinidade, versatilidade, baixa toxicidade, con menos posibilidades de provocar efectos secundarios e a un menor costo.Por outra parte, aínda que a nanotecnoloxía é un campo moi prometedor, non se pode esquecer os numerosos problemas e desafíos que representa a súa utilización. O corpo humano non absorbe ben estos metais, por tanto os seus compostos poden ser tóxicos. Ata o 50% de pacientes con artrose tratados con medicamentos que contiñan ouro sufriron danos hepáticos e renais, se ben é certo que con concentracións en varios órdes de magnitude maiores ás usadas con nanopartículas. No ámbito biomédico, un abano importante de cuestións relativas co procesamento e reproducibilidade das nanopartículas así como aspectos relacionados coa biocompatibilidade, resposta inmune ou seguridade a longo prazo deben ser tamén consideradas. En calquera caso, a necesidade de ofrecer á sociedade unha terapéutica cada vez máis eficaz e con menores riscos permite augurar á nanomedicina un futuro brillante.
 |
O Dr. Hainfeld é profesor na Universidade Stony Brook e no Laboratorio Nacional Brookhaven (Nova York, ademais de presidente da compañía Nanoprobes Inc. (a cal fundou en 1990). Graduouse en Enxeñería Eléctrica na Universidade de Princeton, doctorándose máis tarde en Bioquímica na Universidad de Texas en Austin e seguindo coa súa investigación post-doctoral no campo da Biofísica/Bioloxía na Universidade de Chicago. En 1976 incorporouse ó Departamento de Bioloxía do Laboratorio Nacional de Brookhaven, onde traballou no Scanning Transmission Electron Microscope (STEM Facility) ata o 2009. As súas investigacións actuais céntranse no uso de nanopartículas de ouro magnéticas para o tratamiento do cancro, os usos de nanopartículas metálicas como medios de contraste en radiodiagnóstico con raios-X e resonancia magnética, e o desenvolvemento de novos marcadores para microscopía electrónica. Foi gañador entre outros do premio Röntgen Prize do Instituto Británico de Radioloxía en 2011.
|
Referencias:
- Nanoprobes, Inc.
- Revista Ciencia y Desarrollo xaneiro-febreiro 2014
- Yolanda Prezado, Laboratoire Imagerie et Modelisation pour la Neurobiologie et la Cancérologie (IMNC)-CNRS, ponencia "Nanopartículas y Radioterapia" no III Congreso SEFM-SEPR 2013
- Nanotecnología | Investigación en Galicia, artigo El Mundo, abril 2012
- Científicos de la USC mejoran una técnica contra el cáncer, artigo El Correo Gallego, abril 2013